Uncategorised
Willkommen im Kompetenzzentrum München der SGS-Gruppe. In unseren Testlaboren in Puchheim bei München sowie Gelting und Rosenheim stehen Ihnen auf über 10.000 qm modernste Prüf- und Simulationseinrichtungen zur Verfügung.
Die SGS ist das weltweit führende Unternehmen in den Bereichen Prüfen, Testen, Verifizieren und Zertifizieren.
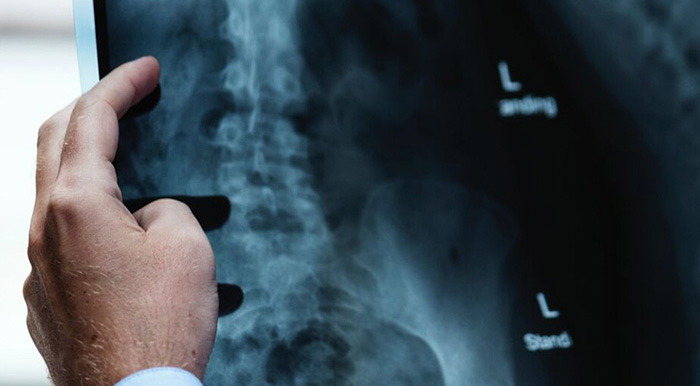
Prüfungen an Geräten und Systemen der Röntgendiagnostik – Anwendung der IEC 60601-1-3 und IEC 60601-2-54
Im Rahmen der Akkreditierungen durch die DAkkS/ILAC (DIN EN ISO/IEC 17025) und des ...
Inspektionsdienstleistungen für elektrische und elektronische Geräte
„Inspektion“ kann im Grunde eine große Vielfalt von unterschiedlichen Dienstleistungen an allen Stationen des Prozesses bedeuten. Von der Evaluierung einer potenziellen Geschäftsbeziehung über die Qualitätskontrolle in laufenden Produktionen ...
Spezifische Absorptionsrate und Messungen der maximal zulässigen Exposition (mpe)
Drahtlose Endgeräte wie 5G, LTE, GSM und GPRS, CDMA, WLAN, Bluetooth und WCDMA, einschließlich Handys und anderer mobiler Geräte, strahlen Hochfrequenzenergie ab. Starke elektrische und magnetische Strahlung ist nachweislich schädlich ...
Benennung nach Medizinprodukteverordnung
Die SGS Fimko Oy ist durch die finnische Behörde FIMEA als Benannte Stelle für die Medizinprodukteverordnung (EU) 2017/745 benannt. Download Benennungsurkunde Finnish Medicins Agency Folgende Konformitätsbewertungsverfahren sind in die Benennung eingeschlossen (Verordnung ...

EMV-Prüfung an Pedelecs und E-Bikes nach EPAC/EMC-Norm EN 15194
E-Bikes und Pedelecs werden als Alternative zur Pkw-Nutzung immer beliebter und müssen hohe gesetzliche Anforderungen an Qualität, ...
Medizinprodukte-Zertifizierung mit SGS – treffen Sie uns auf der RAPS Euro Convergence 2024 im Mai in Berlin
Sie möchten Ihr Medizinprodukt nach MDR prüfen und zertifizieren lassen und dabei nicht durch lange Wartezeiten ausgebremst werden? Sie erwägen als Medizinproduktehersteller einen Wechsel Ihrer Benannten ...
Die SGS beim EMV Kongress in Köln – vom 12. bis 14. März 2024
Auch in diesem Jahr stellen wir mit unseren Fachexperten auf dem EMV Kongress vom 12. - 14. März in Köln folgende Beiträge und Workshops vor: 1. EMV, Funk und Produktsicherheit – Anforderungen für den internationalen Marktzugang Wenn Sie Ihre ...

Lampen / Leuchten / LED – Prüfspektrum Produktsicherheit
Die SGS deckt mit ihrer umfassenden Palette an Akkreditierungen eine Vielzahl von Produktsicherheitsnormen für Lampen, Leuchten und LEDs in ...
Umzug des Standortes München der SGS Germany GmbH von der Hofmannstraße nach Puchheim
Die Niederlassung der SGS Germany GmbH in München, Hofmannstraße zieht aktuell an den neuen Standort Puchheim, Benzstraße im Westen Münchens um. Im Einzelnen betrifft es die akkreditierten Prüfbereiche Elektromagnetische ...
Die SGS auf der Fachtagung (online) des MDR COMPETENCE - Netzwerks 2023
Die zweite Fachtagung des MDR COMPETENCE - Netzwerks findet am 07. Dezember online mit spannenden Vorträgen zum Thema Verifikation & Validierung in der Produktkonformitätsbewertung für Medizintechnik statt. Zahlreiche Experten geben dort ...
Medizinprodukte: Prüfung & Zertifizierung mit SGS – treffen Sie uns auf der medica 2023
Sie möchten Ihr Medizinprodukt nach MDR prüfen und zertifizieren lassen und dabei nicht durch lange Wartezeiten ausgebremst werden oder erwägen als Medizinproduktehersteller einen Wechsel Ihrer Benannten Stelle? Profitieren ...
SGS Fimko veröffentlicht ihr erstes MDR-Zertifikat für deutschen Hersteller
Wir freuen uns bekannt zu geben, dass die Benannte Stelle SGS Fimko (CE0598) nun auch ihr erstes MDR-Zertifikat für einen Medizintechnikhersteller in Deutschland ausgestellt hat. Die Gründler GmbH in Freudenstadt (Baden-Württemberg) ist ...
Neue IMDRF-Veröffentlichung: Leitlinie zum Inhalt von regulatorischen Bewertungsberichten für Medizinprodukte
Das Internationale Forum der Aufsichtsbehörden für Medizinprodukte (IMDRF) ist eine freiwillige Gruppe von Regulierungsbehörden für Medizinprodukte aus aller Welt, die sich 2011 konstituiert hat und auf ...
Leitfaden zur Umsetzung der Vigilanzanforderungen der Medizingeräteverordnung (EU) 2017/745 veröffentlicht: Fragen und Antworten zu Begriffen und Konzepten der Vigilanz
Die Koordinierungsgruppe Medizinprodukte (MDCG) hat den neuen Leitfaden MDCG 2023-3 mit dem Titel „Fragen und Antworten zu Vigilanzbegriffen und ...
Die SGS beim EMV-Kongress 2023 in Stuttgart – 28. bis 30.03.23
Auch 2023 stellen wir mit unseren Fachexperten Armin Hudetz, Josef Bauer, Markus Spiel und Michael Sperling vom 28. bis 30.03. auf dem EMV-Kongress in Stuttgart interessante Workshops vor. In diesem Jahr bieten wir Ihnen drei Beiträge an: 1.) EMV, Funk ...
Update: Liste der harmonisierten Normen unter der Medizinprodukteverordnung (MDR)
Die Liste der harmonisierten Normen unter der Medizinprodukteverordnung (EU) 2017/745 wurde um die neuesten normativen Dokumente für Beatmungsgeräte und sterile Medizinprodukte ergänzt. Die Frist für die Anwendung der Normen durch die ...
Update der Quality System Regulation mit den Anforderungen der ISO 13485:2016
Die United States General Services Administration hat kürzlich angekündigt, dass die FDA die bestehende „Quality System Regulation“ für Medizinprodukte mit den Anforderungen der ISO 13485:2016 aktualisieren wird: Veröffentlichung ...
Offenlegung von Standardgebühren der Benannten Stellen
Die Medical Device Coordination Group (MDCG) empfiehlt allen Benannten Stellen für MDR-Zertifizierungen, die Standardgebühren offenzulegen. „Sie sollten direkt und einfach auf der Website der Benannten Stelle ohne zusätzliche Schritte zugänglich sein“, ...
Die Frist für die MDR-Zertifizierung wurde verlängert: Wie geht es weiter?
Am 6. Januar 2023 hat die EU-Kommission einen Vorschlag angenommen, der mehr Zeit für die Zertifizierung von Medizinprodukten gemäß der Verordnung (EU) 2017/745 gewährt. Diese Entscheidung zielte darauf ab, das Risiko von Engpässen bei ...
Produkte ohne medizinischen Verwendungszweck nach MDR (EU) 2017/745 Anhang XVI
Die Europäische Kommission hat zwei neue Dokumente veröffentlicht, in denen die Regeln für den EU-Marktzugang für Hersteller von Produkten ohne medizinische Zweckbestimmung detailliert beschrieben werden. Gemeinsame Spezifikationen ...